Plynný dusík nalézá využití jako inertní atmosféra např. v prostředí, kde hrozí nebezpečí výbuchu, pro svařování v inertní atmosféře (TIG), při výrobě integrovaných obvodů, nerezové oceli. Používá se také k plnění obalů, aby se výrobky nezmačkaly a nezvlhly – například brambůrky v sáčku.Dusík má, podobně jako C a O, schopnost tvořit násobné vazby prostřednictvím interakcí pπ–pπ s jiným atomem N nebo s atomem C či O. Vaznost dusíku je maximálně 4, i když jsou známy struktury, ve kterých má atom N koordinační číslo 6 nebo 8.Pokud aplikace potřebuje dusík, existují tři hlavní způsoby, jak získat plyn. Prvním je pronajata nádrž na dusík na místě a dodávka plynu. Druhým je plynný dusík ve vysokotlakých lahvích. Poslední možností je produkovat dusík pomocí stlačeného vzduchu.
Co je těžší dusík nebo kyslík : O bodu varu rozhodují zejména hmotnost atomů či molekul dané látky a poté interakce mezi nimi. Protože kyslík má těžší molekulu než dusík, bude mít vyšší tva bude tedy destilovat později.
Jak funguje dusík
Dusík je nehořlavý plyn tvořící 78 % zemské atmosféry. Dusík je vyhledávaný pro své inertními vlastnosti. Ve své plynné formě vytěsňuje vzduch, a tudíž snižuje nebo eliminuje oxidaci materiálů. Používá se také jako pomocný plyn při řezání laserem.
Co dělá dusík v těle : Dusík je sice základní složkou atmosféry, ale při zvýšené koncentraci, kdy způsobí vytěsnění kyslíku, dojde u člověka k bolestem hlavy a celkovému kolapsu organismu.
Čím doplnit dusík
Zlepšení růstu brzděného nedostatkem dusíku lze nejrychleji dosáhnout mimokořenovou výživou roztokem močoviny. Pokud jsou listy již silně poškozeny, je jistější hnojivá zálivka roztokem ledku vápenatého. Dusík má pět valenčních elektronů a u jednoduchých aminů je trojvazný, přičemž dva elektrony nevyužité k tvorbě vazeb vytváří volný elektronový pár. Prostřednictvím tohoto páru může dusík vytvořit další vazbu s atomem vodíku, čímž se stane čtyřvazným a získá kladný náboj; vzniklá částice se nazývá amonný kation.
Co způsobuje dusík
Ačkoli je dusík netoxický a inertní, může ve vysokých koncentracích způsobit dušení z nedostatku kyslíku. Kromě toho kontakt s kapalným produktem může způsobit chladové a mrazové popáleniny.Proč zůstal propan ve sklenici a neutekl nahoru (Propan je těžší než vzduch. 1 litr vzduchu váží za normálního tlaku při pokojové teplotě přibližně 1,2 g, 1 litr propanu za stejných podmínek 1,7 g.)Je chemicky stejný jako plynný dusík, ovšem ve formě kapaliny. Je kapalný i při normálním (atmosférickém) tlaku. Jeho teplota je – 196°C, za této teploty se také vaří a tedy i odpařuje. Přihnojování dusíkem se provádí rychle rozpustnými formami dusíku (ledek, močovina), základní hnojení pak pevnými a pomalu rozpustnými formami, které zapravujeme do půdy. Nejnáročnější na dusík jsou košťáloviny a plodová zelenina, navíc tyto rostliny zůstávají na záhonech dlouho a proto z půdy živiny odčerpají.
Kde najdeme dusík : Volný dusík se vyskytuje v podobě dvouatomových molekul. Jedná se o nejrozšířenější plyn v zemské atmosféře (78 %), také je vázán v celé řadě přírodních sloučenin (např soli kys. dusičné). Dusík je také významným biogenním prvkem – je součástí všech živých organizmů (živočichů i rostlin).
Jak se projevuje nedostatek dusíku : Charakteristickými příznaky deficitu N jsou omezený vzrůst, menší listy a bledě zelené až žlutavé zbarvení listů. Symptomy jsou nejdříve rozpoznatelné na starších listech, které žloutnou a bělají s postupujícím deficitem. Extrémní deficit N způsobuje předčasné stárnutí a zmenšení klasů.
Kdy hnojit dusíkatým vápnem
Základní hnojení (nad 50 g/m2) 2 až 3 týdny před setím či výsadbou, kdy dusíkaté vápno rozhodíme na plochu a zapravíme. při aplikaci by měla být půda vlhká. Hnojivo je určené především k dezinfekci půdy před výsadbou a dále pro obnovu trávníku a k urychlení zrání kompostu, k použití i na podzim. Molekuly dusíku jsou tvořeny dvěma atomy, mezi kterými je trojná vazba. Tato trojná vazba je velice pevná a díky ní je molekula N2 málo reaktivní.Vodík je nejlehčí a nejjednodušší plynný chemický prvek a tvoří převážnou část hmoty ve vesmíru.
Který plyn je jedovatý : Oxid uhelnatý (Carbonmonooxid, CO) je silně jedovatý plyn, který se uvolňuje při spalování paliv. Je neviditelný, bez zápachu a proto je velmi obtížně zjistitelný lidskými smysly. Oxid uhelnatý se vdechováním váže na červené krevní barvivo hemoglobin (vzniká karbonylhemoglobin) asi 220 krát lépe než kyslík.
Antwort Jak se vytvari dusík? Weitere Antworten – Jak se využívá dusík
Plynný dusík nalézá využití jako inertní atmosféra např. v prostředí, kde hrozí nebezpečí výbuchu, pro svařování v inertní atmosféře (TIG), při výrobě integrovaných obvodů, nerezové oceli. Používá se také k plnění obalů, aby se výrobky nezmačkaly a nezvlhly – například brambůrky v sáčku.Dusík má, podobně jako C a O, schopnost tvořit násobné vazby prostřednictvím interakcí pπ–pπ s jiným atomem N nebo s atomem C či O. Vaznost dusíku je maximálně 4, i když jsou známy struktury, ve kterých má atom N koordinační číslo 6 nebo 8.Pokud aplikace potřebuje dusík, existují tři hlavní způsoby, jak získat plyn. Prvním je pronajata nádrž na dusík na místě a dodávka plynu. Druhým je plynný dusík ve vysokotlakých lahvích. Poslední možností je produkovat dusík pomocí stlačeného vzduchu.
Co je těžší dusík nebo kyslík : O bodu varu rozhodují zejména hmotnost atomů či molekul dané látky a poté interakce mezi nimi. Protože kyslík má těžší molekulu než dusík, bude mít vyšší tva bude tedy destilovat později.
Jak funguje dusík
Dusík je nehořlavý plyn tvořící 78 % zemské atmosféry. Dusík je vyhledávaný pro své inertními vlastnosti. Ve své plynné formě vytěsňuje vzduch, a tudíž snižuje nebo eliminuje oxidaci materiálů. Používá se také jako pomocný plyn při řezání laserem.
Co dělá dusík v těle : Dusík je sice základní složkou atmosféry, ale při zvýšené koncentraci, kdy způsobí vytěsnění kyslíku, dojde u člověka k bolestem hlavy a celkovému kolapsu organismu.
Čím doplnit dusík
Zlepšení růstu brzděného nedostatkem dusíku lze nejrychleji dosáhnout mimokořenovou výživou roztokem močoviny. Pokud jsou listy již silně poškozeny, je jistější hnojivá zálivka roztokem ledku vápenatého.

Dusík má pět valenčních elektronů a u jednoduchých aminů je trojvazný, přičemž dva elektrony nevyužité k tvorbě vazeb vytváří volný elektronový pár. Prostřednictvím tohoto páru může dusík vytvořit další vazbu s atomem vodíku, čímž se stane čtyřvazným a získá kladný náboj; vzniklá částice se nazývá amonný kation.
Co způsobuje dusík
Ačkoli je dusík netoxický a inertní, může ve vysokých koncentracích způsobit dušení z nedostatku kyslíku. Kromě toho kontakt s kapalným produktem může způsobit chladové a mrazové popáleniny.Proč zůstal propan ve sklenici a neutekl nahoru (Propan je těžší než vzduch. 1 litr vzduchu váží za normálního tlaku při pokojové teplotě přibližně 1,2 g, 1 litr propanu za stejných podmínek 1,7 g.)Je chemicky stejný jako plynný dusík, ovšem ve formě kapaliny. Je kapalný i při normálním (atmosférickém) tlaku. Jeho teplota je – 196°C, za této teploty se také vaří a tedy i odpařuje.

Přihnojování dusíkem se provádí rychle rozpustnými formami dusíku (ledek, močovina), základní hnojení pak pevnými a pomalu rozpustnými formami, které zapravujeme do půdy. Nejnáročnější na dusík jsou košťáloviny a plodová zelenina, navíc tyto rostliny zůstávají na záhonech dlouho a proto z půdy živiny odčerpají.
Kde najdeme dusík : Volný dusík se vyskytuje v podobě dvouatomových molekul. Jedná se o nejrozšířenější plyn v zemské atmosféře (78 %), také je vázán v celé řadě přírodních sloučenin (např soli kys. dusičné). Dusík je také významným biogenním prvkem – je součástí všech živých organizmů (živočichů i rostlin).
Jak se projevuje nedostatek dusíku : Charakteristickými příznaky deficitu N jsou omezený vzrůst, menší listy a bledě zelené až žlutavé zbarvení listů. Symptomy jsou nejdříve rozpoznatelné na starších listech, které žloutnou a bělají s postupujícím deficitem. Extrémní deficit N způsobuje předčasné stárnutí a zmenšení klasů.
Kdy hnojit dusíkatým vápnem
Základní hnojení (nad 50 g/m2) 2 až 3 týdny před setím či výsadbou, kdy dusíkaté vápno rozhodíme na plochu a zapravíme. při aplikaci by měla být půda vlhká. Hnojivo je určené především k dezinfekci půdy před výsadbou a dále pro obnovu trávníku a k urychlení zrání kompostu, k použití i na podzim.
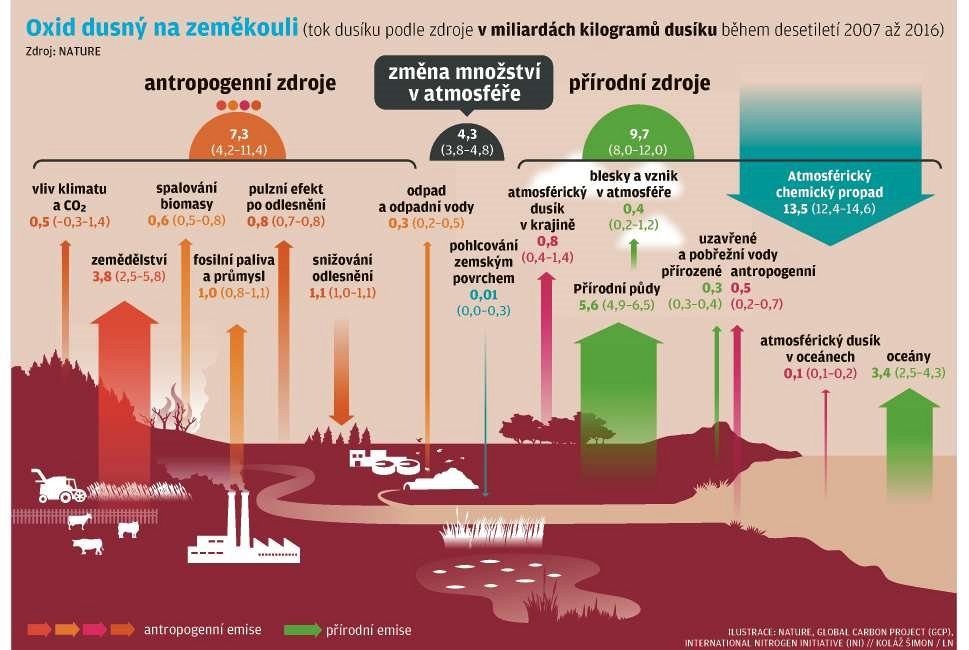
Molekuly dusíku jsou tvořeny dvěma atomy, mezi kterými je trojná vazba. Tato trojná vazba je velice pevná a díky ní je molekula N2 málo reaktivní.Vodík je nejlehčí a nejjednodušší plynný chemický prvek a tvoří převážnou část hmoty ve vesmíru.
Který plyn je jedovatý : Oxid uhelnatý (Carbonmonooxid, CO) je silně jedovatý plyn, který se uvolňuje při spalování paliv. Je neviditelný, bez zápachu a proto je velmi obtížně zjistitelný lidskými smysly. Oxid uhelnatý se vdechováním váže na červené krevní barvivo hemoglobin (vzniká karbonylhemoglobin) asi 220 krát lépe než kyslík.