Anionty většinou vznikají z elektronegativních prvků, například kyslíku, síry, dusíku nebo halogenů: N + 3 e− → N3−.Kationty a anionty
Pokud neutrální atom přijde o jeden nebo více elektronů, celkový počet elektronů se sníží, zatímco počet protonů v jádře zůstává stejný. Dojde k tomu, že se z atomu stává kation, tedy ion s kladným nábojem.Kationty jsou kladně nabité, počet elektronů v nich je nižší než počet protonů. Anionty jsou záporně nabité, počet elektronů v nich je vyšší než počet protonů.
Kolik vazeb prvek tvoří : Podle toho, kolik chemických vazeb je atom prvku schopen vytvořit, hovoříme o vaznosti prvku. Prvky ve sloučeninách mohou být maximálně osmivazné. Pro elektrony je z energetického hlediska výhodné tvořit páry.
Jak vznikají kationty
Atom přijímající elektrony je elektronegativní, má velkou elektronovou afinitu a bývá to často nekov. Ion M e X n + nese kladný náboj a nazývá se kation. Kation prvku vzniká tak, že elektricky neutrální atom ztratí jeden nebo více elektronů: M e − n e X − ⟶ M e X n + , např. C a − 2 e X − ⟶ C a X 2 + .
Jak vznikají kationty a anionty : Iont vzniká tak, že atom přijme nebo odevzdá elektrony tj., kdy počet protonů a elektronů není stejný. Kationt je iont, který má méně elektronů než protonů. Aniont je iont, který má naopak více elektronů než protonů. Toto video z fyziky je určeno zejména pro žáky základní školy.
Iont vzniká tak, že atom přijme nebo odevzdá elektrony tj., kdy počet protonů a elektronů není stejný. Kationt je iont, který má méně elektronů než protonů. Aniont je iont, který má naopak více elektronů než protonů. Toto video z fyziky je určeno zejména pro žáky základní školy. Kation (někdy psáno i ve tvaru „kationt“) je atom nebo molekula, která má kladný elektrický náboj (+). Příklady látek, které se v lidském těle vyskytují ve formě kationtů, jsou sodík (Na+), draslík (K+), vápník (Ca2+), hořčík (Mg2+), železo (Fe2+, Fe3+) či zinek (Zn2+).
Jak poznat kolik má prvek valenčních elektronů
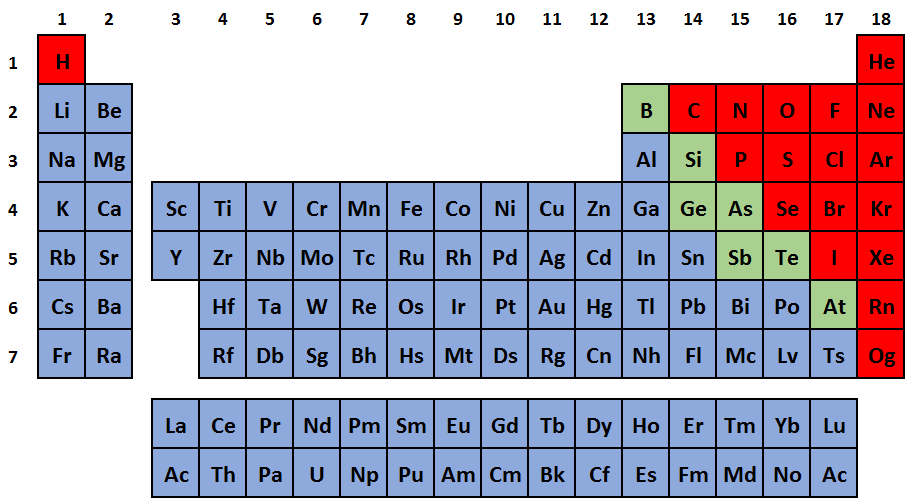
Obecně platí, že počet valenčních elektronů je stejný jako číslo sloupce a roste v rámci řádku zleva doprava. Prvky skupiny 1 mají jeden valenční elektron a prvky skupiny 18 mají osm valenčních elektronů až na helium, které má celkem pouze dva elektrony.Počet elektronů je stejný jako počet protonů. Atom, který má v jádru pět protonů, má v atomovém obalu 5 elektronů. Prvek, který má v jádru pět protonů se nazývá BOR a má značku B. Prvek, který má v jádru osm protonů se nazývá KYSLÍK a má značku O.Molekula se skládá z atomů a je elektroneutrální (nenese elektrický náboj). Je charakterizovaná určitým složením (druh a počet přítomných atomů) a strukturou (jejich vzájemné prostorové uspořádání, způsob vazeb). Molekuly prvků obsahují stejné atomy, např. H2, O2, O3, N2. Amoniak vzniká reakcí amonných solí se silnými hydroxidy, např. působením hydroxidu sodného na chlorid amonný: NH4Cl + NaOH → NH3 + NaCl + H2O.
Jak vznika kationt a aniont : Iont vzniká tak, že atom přijme nebo odevzdá elektrony tj., kdy počet protonů a elektronů není stejný. Kationt je iont, který má méně elektronů než protonů. Aniont je iont, který má naopak více elektronů než protonů. Toto video z fyziky je určeno zejména pro žáky základní školy.
Jak vypadá kationt : Kation (někdy psáno i ve tvaru „kationt“) je atom nebo molekula, která má kladný elektrický náboj (+). Příklady látek, které se v lidském těle vyskytují ve formě kationtů, jsou sodík (Na+), draslík (K+), vápník (Ca2+), hořčík (Mg2+), železo (Fe2+, Fe3+) či zinek (Zn2+).
Jaký prvek má 8 elektronů
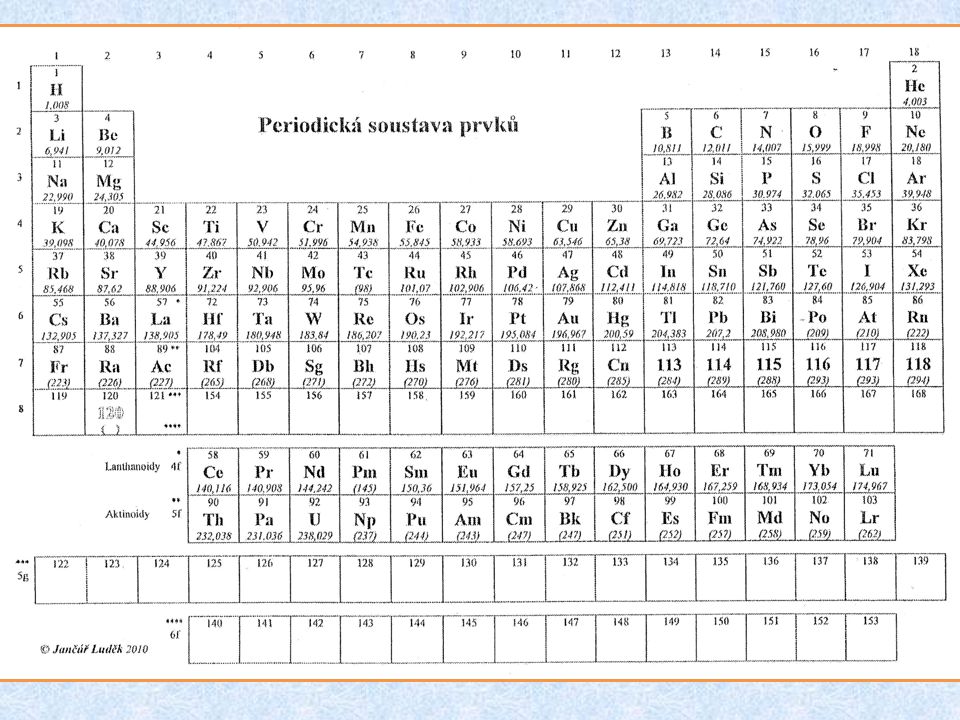
V této tabulce vidíme, že helium má zcela zaplněnou valenční slupku, tedy dva elektrony v své první a jediné slupce 1n. Podobně je tomu u neonu, který má osm elektronů v jeho valenční slupce 2n. Tyto elektronové konfigurace jsou zodpovědné za to, že helium a neon jsou velmi stabilní. Prvky s a p se také nazývají nepřechodné prvky, jejich valenční elektrony (nebo orbitaly) jsou pouze v jediné – poslední vrstvě (slupce) obalu atomu – jde o skupiny I.A (1) až VIII.A (17) a počet valenčních elektronů (orbitalů) těchto prvků odpovídá číslu skupiny.Protonové číslo kyslíku je 8, a proto jádro atomu kyslíku obsahuje 8 protonů, elektronový obal 8 elektronů.
Který prvek má 12 protonů : Seznam všech objevených prvků
Antwort Jaký prvek snadno tvoří kationty? Weitere Antworten – Které prvky tvoří anionty
Anionty většinou vznikají z elektronegativních prvků, například kyslíku, síry, dusíku nebo halogenů: N + 3 e− → N3−.Kationty a anionty
Pokud neutrální atom přijde o jeden nebo více elektronů, celkový počet elektronů se sníží, zatímco počet protonů v jádře zůstává stejný. Dojde k tomu, že se z atomu stává kation, tedy ion s kladným nábojem.Kationty jsou kladně nabité, počet elektronů v nich je nižší než počet protonů. Anionty jsou záporně nabité, počet elektronů v nich je vyšší než počet protonů.
Kolik vazeb prvek tvoří : Podle toho, kolik chemických vazeb je atom prvku schopen vytvořit, hovoříme o vaznosti prvku. Prvky ve sloučeninách mohou být maximálně osmivazné. Pro elektrony je z energetického hlediska výhodné tvořit páry.
Jak vznikají kationty
Atom přijímající elektrony je elektronegativní, má velkou elektronovou afinitu a bývá to často nekov. Ion M e X n + nese kladný náboj a nazývá se kation. Kation prvku vzniká tak, že elektricky neutrální atom ztratí jeden nebo více elektronů: M e − n e X − ⟶ M e X n + , např. C a − 2 e X − ⟶ C a X 2 + .
Jak vznikají kationty a anionty : Iont vzniká tak, že atom přijme nebo odevzdá elektrony tj., kdy počet protonů a elektronů není stejný. Kationt je iont, který má méně elektronů než protonů. Aniont je iont, který má naopak více elektronů než protonů. Toto video z fyziky je určeno zejména pro žáky základní školy.
Iont vzniká tak, že atom přijme nebo odevzdá elektrony tj., kdy počet protonů a elektronů není stejný. Kationt je iont, který má méně elektronů než protonů. Aniont je iont, který má naopak více elektronů než protonů. Toto video z fyziky je určeno zejména pro žáky základní školy.

Kation (někdy psáno i ve tvaru „kationt“) je atom nebo molekula, která má kladný elektrický náboj (+). Příklady látek, které se v lidském těle vyskytují ve formě kationtů, jsou sodík (Na+), draslík (K+), vápník (Ca2+), hořčík (Mg2+), železo (Fe2+, Fe3+) či zinek (Zn2+).
Jak poznat kolik má prvek valenčních elektronů
Obecně platí, že počet valenčních elektronů je stejný jako číslo sloupce a roste v rámci řádku zleva doprava. Prvky skupiny 1 mají jeden valenční elektron a prvky skupiny 18 mají osm valenčních elektronů až na helium, které má celkem pouze dva elektrony.Počet elektronů je stejný jako počet protonů. Atom, který má v jádru pět protonů, má v atomovém obalu 5 elektronů. Prvek, který má v jádru pět protonů se nazývá BOR a má značku B. Prvek, který má v jádru osm protonů se nazývá KYSLÍK a má značku O.Molekula se skládá z atomů a je elektroneutrální (nenese elektrický náboj). Je charakterizovaná určitým složením (druh a počet přítomných atomů) a strukturou (jejich vzájemné prostorové uspořádání, způsob vazeb). Molekuly prvků obsahují stejné atomy, např. H2, O2, O3, N2.
Amoniak vzniká reakcí amonných solí se silnými hydroxidy, např. působením hydroxidu sodného na chlorid amonný: NH4Cl + NaOH → NH3 + NaCl + H2O.
Jak vznika kationt a aniont : Iont vzniká tak, že atom přijme nebo odevzdá elektrony tj., kdy počet protonů a elektronů není stejný. Kationt je iont, který má méně elektronů než protonů. Aniont je iont, který má naopak více elektronů než protonů. Toto video z fyziky je určeno zejména pro žáky základní školy.
Jak vypadá kationt : Kation (někdy psáno i ve tvaru „kationt“) je atom nebo molekula, která má kladný elektrický náboj (+). Příklady látek, které se v lidském těle vyskytují ve formě kationtů, jsou sodík (Na+), draslík (K+), vápník (Ca2+), hořčík (Mg2+), železo (Fe2+, Fe3+) či zinek (Zn2+).
Jaký prvek má 8 elektronů
V této tabulce vidíme, že helium má zcela zaplněnou valenční slupku, tedy dva elektrony v své první a jediné slupce 1n. Podobně je tomu u neonu, který má osm elektronů v jeho valenční slupce 2n. Tyto elektronové konfigurace jsou zodpovědné za to, že helium a neon jsou velmi stabilní.

Prvky s a p se také nazývají nepřechodné prvky, jejich valenční elektrony (nebo orbitaly) jsou pouze v jediné – poslední vrstvě (slupce) obalu atomu – jde o skupiny I.A (1) až VIII.A (17) a počet valenčních elektronů (orbitalů) těchto prvků odpovídá číslu skupiny.Protonové číslo kyslíku je 8, a proto jádro atomu kyslíku obsahuje 8 protonů, elektronový obal 8 elektronů.
Který prvek má 12 protonů : Seznam všech objevených prvků