Síra hoří na vzduchu modrým plamenem za vzniku oxidu siřičitého SO2 a v malém množství i oxidu sírového SO3.Oxid siřičitý je i přes všechny své benefity stále jedovatý plyn, který i v malém množství vyvolává u citlivých lidí alergické reakce, závratě, bolesti hlavy a břicha, problémy astmatického typu. Studie, která testovala účinky SO2 na zvířatech, potvrdila výskyt žaludečních vředů po požití této chemikálie.Oxid sírový vzniká přirozeně oxidací oxidu siřičitého a v plynné fázi je hlavní příčinou vzniku tzv. kyselých dešťů, které vedly koncem 20.
Co obsahuje Siričitany : – působí jako pomocný prostředek (řepný cukr). Obsah siřičitanů v potravinách se pohybuje v rozmezí do 10 mg/kg (např. zmrazená těsta, kukuřičný sirup, rosoly), do 60 mg/kg (čerství garnáti, nakládaná zelenina v nálevu, čerstvé houby), do 100 mg/kg (např. sušené brambory, vinný ocet).
Co vzniká při hoření
Hoření je fyzikálně chemická reakce, při které hořlavá látka reaguje vysokou rychlostí s oxidačním prostředkem za vzniku tepla a světla. Je to reakce exotermická. Při této reakci vzniká teplo, světlo (plamen) a produkty hoření (kouř).
Jak je citit síra : Většina z nás si pod slovem síra představí nepříjemný zápach připomínající zkažená vejce či chemickou laboratoř. Síra je ale především minerál, který je důležitý pro lidský organismus a naše zdraví.
Síra hoří namodralým plamenem a při hoření uvolňuje čpavý kysličník siřičitý. Této vlastnosti si lidé všimli už ve starověku a používali síru k rozličným účelům. Oxid siřičitý se vyskytuje v sopečných plynech a rozpuštěný jako kyselina siřičitá v podzemních (minerálních) vodách ve vulkanicky aktivních oblastech.
Co tvoří oxidy
Binární (dvouprvkové) sloučeniny kyslíku s dalším prvkem se nazývají oxidy. Dříve se používal název kysličník. Oxidy obsahují ve své molekule oxidový anion O2-. Oxidy vznikají odtržením 2 atomů vodíku z vody (H2O).Oxid siřičitý je jedovatý a vysoce dráždivý, často zmiňovaný jako znečišťovatel ovzduší. Jedná se o plyn vznikající hořením síry. Oxid siřičitý je antioxidant, konzervant a prostředek proti hnědnutí.Po přiklopení svíčky sklenicí či odměrným válcem začne plamen zahřívat vzduch v nádobě. Vzduch se přitom rozpíná a ve formě bublinek může unikat kolem spodního okraje nádoby. Při hoření se v nádobě slučuje kyslík s uhlovodíky obsaženými ve svíčce a vzniká vodní pára a oxid uhličitý. čpavek, fenoly, kyanidy, dehet. jsou obohaceny různými látkami, jako jsou změkčovadla, barviva a stabilizátory. Obsahují často těžké kovy, které se při spalování jednak uvolňují do ovzduší a jednak zůstávají v popelu.
Co způsobuje Smradlave prdy : Mezi nadýmavé potraviny patří luštěniny, košťálová zelenina, cibule, česnek, silně kořeněná jídla, sycené vody, kynuté pečivo, obzvláště to čerstvě upečené a alkohol, především víno. Tyto potraviny jsou bohaté na síru, která ovlivňuje střevní bakterie a vzniká sirovodík páchnoucí po shnilých vejcích.
Co zpusobuje síra : Síra má tzv. keratolytický efekt. To ve zkratce znamená, že snižuje množství šupin na povrchu lidské pokožky, odstraňuje zrohovatělé odumřelé kožní buňky a má výrazně pozitivní vliv na kvalitu pojivové tkáně a chrupavek. Blokuje totiž odbourávání elastinu a kolagenu v chrupavkách.
Jak se vyrábí síra
Jako zdroj pro průmyslovou výrobu elementární síry slouží zejména přírodní síra, sulfidy a sírany. Dále se využívá síra přítomná ve formě organických i anorganických sloučenin v zemním plynu, ropě a uhlí. A. Elementární síra se z vytěžené horniny nejčastěji vytavuje přehřátou vodní párou. Oxid siřičitý je bezbarvý reaktivní dráždivý plyn, snadno rozpustný ve vodě. Zdrojem emisí do ovzduší jsou hlavně elektrárny a doprava.Oxidy mohou vznikat buď prudkou oxidací (hořením) za přítomnosti kyslíku anebo pozvolnou oxidací jiným způsobem, zejména kyslíkem atmosférickým anebo kyslíkem obsaženým v některých látkách (oxidačních činidlech), a při dalších chemických reakcích. Kyslík má v oxidech oxidační číslo −II.
Jak vzniká oxidace : materiál + kyslík + energie = oxid materiálu. Je-li tato energie kladná, pak materiál je stabilní; v případě záporné hodnoty energie bude docházet k samovolné oxidaci.
Antwort CO vznika hořením síry? Weitere Antworten – Co vzniká hořením síry
Síra hoří na vzduchu modrým plamenem za vzniku oxidu siřičitého SO2 a v malém množství i oxidu sírového SO3.Oxid siřičitý je i přes všechny své benefity stále jedovatý plyn, který i v malém množství vyvolává u citlivých lidí alergické reakce, závratě, bolesti hlavy a břicha, problémy astmatického typu. Studie, která testovala účinky SO2 na zvířatech, potvrdila výskyt žaludečních vředů po požití této chemikálie.Oxid sírový vzniká přirozeně oxidací oxidu siřičitého a v plynné fázi je hlavní příčinou vzniku tzv. kyselých dešťů, které vedly koncem 20.
Co obsahuje Siričitany : – působí jako pomocný prostředek (řepný cukr). Obsah siřičitanů v potravinách se pohybuje v rozmezí do 10 mg/kg (např. zmrazená těsta, kukuřičný sirup, rosoly), do 60 mg/kg (čerství garnáti, nakládaná zelenina v nálevu, čerstvé houby), do 100 mg/kg (např. sušené brambory, vinný ocet).
Co vzniká při hoření
Hoření je fyzikálně chemická reakce, při které hořlavá látka reaguje vysokou rychlostí s oxidačním prostředkem za vzniku tepla a světla. Je to reakce exotermická. Při této reakci vzniká teplo, světlo (plamen) a produkty hoření (kouř).
Jak je citit síra : Většina z nás si pod slovem síra představí nepříjemný zápach připomínající zkažená vejce či chemickou laboratoř. Síra je ale především minerál, který je důležitý pro lidský organismus a naše zdraví.
Síra hoří namodralým plamenem a při hoření uvolňuje čpavý kysličník siřičitý. Této vlastnosti si lidé všimli už ve starověku a používali síru k rozličným účelům.
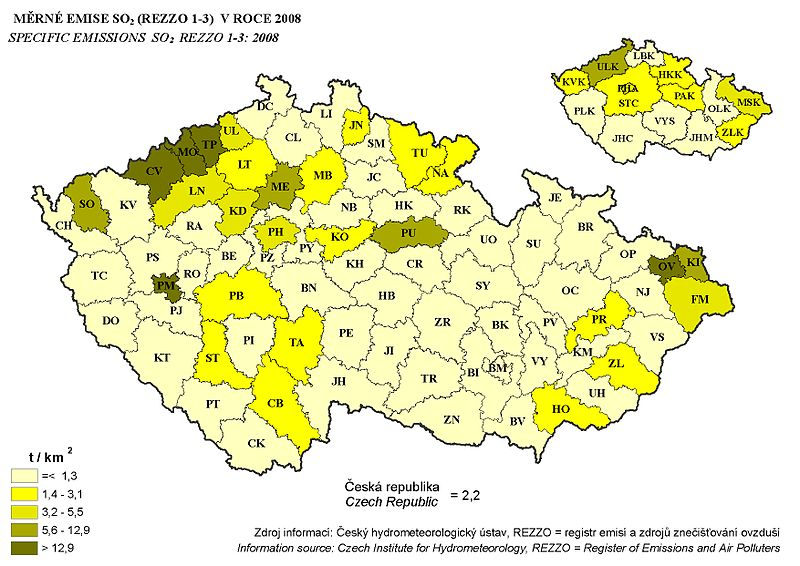
Oxid siřičitý se vyskytuje v sopečných plynech a rozpuštěný jako kyselina siřičitá v podzemních (minerálních) vodách ve vulkanicky aktivních oblastech.
Co tvoří oxidy
Binární (dvouprvkové) sloučeniny kyslíku s dalším prvkem se nazývají oxidy. Dříve se používal název kysličník. Oxidy obsahují ve své molekule oxidový anion O2-. Oxidy vznikají odtržením 2 atomů vodíku z vody (H2O).Oxid siřičitý je jedovatý a vysoce dráždivý, často zmiňovaný jako znečišťovatel ovzduší. Jedná se o plyn vznikající hořením síry. Oxid siřičitý je antioxidant, konzervant a prostředek proti hnědnutí.Po přiklopení svíčky sklenicí či odměrným válcem začne plamen zahřívat vzduch v nádobě. Vzduch se přitom rozpíná a ve formě bublinek může unikat kolem spodního okraje nádoby. Při hoření se v nádobě slučuje kyslík s uhlovodíky obsaženými ve svíčce a vzniká vodní pára a oxid uhličitý.

čpavek, fenoly, kyanidy, dehet. jsou obohaceny různými látkami, jako jsou změkčovadla, barviva a stabilizátory. Obsahují často těžké kovy, které se při spalování jednak uvolňují do ovzduší a jednak zůstávají v popelu.
Co způsobuje Smradlave prdy : Mezi nadýmavé potraviny patří luštěniny, košťálová zelenina, cibule, česnek, silně kořeněná jídla, sycené vody, kynuté pečivo, obzvláště to čerstvě upečené a alkohol, především víno. Tyto potraviny jsou bohaté na síru, která ovlivňuje střevní bakterie a vzniká sirovodík páchnoucí po shnilých vejcích.
Co zpusobuje síra : Síra má tzv. keratolytický efekt. To ve zkratce znamená, že snižuje množství šupin na povrchu lidské pokožky, odstraňuje zrohovatělé odumřelé kožní buňky a má výrazně pozitivní vliv na kvalitu pojivové tkáně a chrupavek. Blokuje totiž odbourávání elastinu a kolagenu v chrupavkách.
Jak se vyrábí síra
Jako zdroj pro průmyslovou výrobu elementární síry slouží zejména přírodní síra, sulfidy a sírany. Dále se využívá síra přítomná ve formě organických i anorganických sloučenin v zemním plynu, ropě a uhlí. A. Elementární síra se z vytěžené horniny nejčastěji vytavuje přehřátou vodní párou.

Oxid siřičitý je bezbarvý reaktivní dráždivý plyn, snadno rozpustný ve vodě. Zdrojem emisí do ovzduší jsou hlavně elektrárny a doprava.Oxidy mohou vznikat buď prudkou oxidací (hořením) za přítomnosti kyslíku anebo pozvolnou oxidací jiným způsobem, zejména kyslíkem atmosférickým anebo kyslíkem obsaženým v některých látkách (oxidačních činidlech), a při dalších chemických reakcích. Kyslík má v oxidech oxidační číslo −II.
Jak vzniká oxidace : materiál + kyslík + energie = oxid materiálu. Je-li tato energie kladná, pak materiál je stabilní; v případě záporné hodnoty energie bude docházet k samovolné oxidaci.