Endotermická (endotermní) reakce (z řeckého ἔξω endo „dovnitř“ a θερμός thermós „teplý, horký, vyhřívaný“) je chemická reakce, při níž se energie spotřebovává, obvykle ve formě tepla. Produkty reakce proto mají vyšší chemickou energii než reaktanty, které do reakce vstoupily.Exotermická (exotermní) reakce (z řeckého ἔξω exo „venku“ a θερμός thermós „teplý, horký, vyhřívaný“) je chemická reakce, při níž se uvolňuje energie, obvykle ve formě tepla. Produkty reakce proto mají nižší chemickou energii než reaktanty, které do reakce vstoupily.Exotermní reakce
Jestliže se při chemické reakci uvolňuje teplo, hovoříme o reakci exotermní (exotermické). Exotermní reakce jsou mnohdy doprovázeny světelnými efekty či prudkým zvýšením teploty reakční směsi. Tyto reakce probíhají většinou samovolně, jejich nejběžnějším příkladem je hoření.
Jaké jsou typy chemických reakcí : Chemické reakce lze klasifikovat podle různých kritérií, včetně fyzikálního stavu substrátů a produktů nebo energetického účinku. Nejčastěji se však dělí podle typu a počtu složek, které se na nich podílejí a podle toho rozlišujeme reakce syntézní, rozkladné a vytěsňovací.
Jak se pozná Endotermická reakce
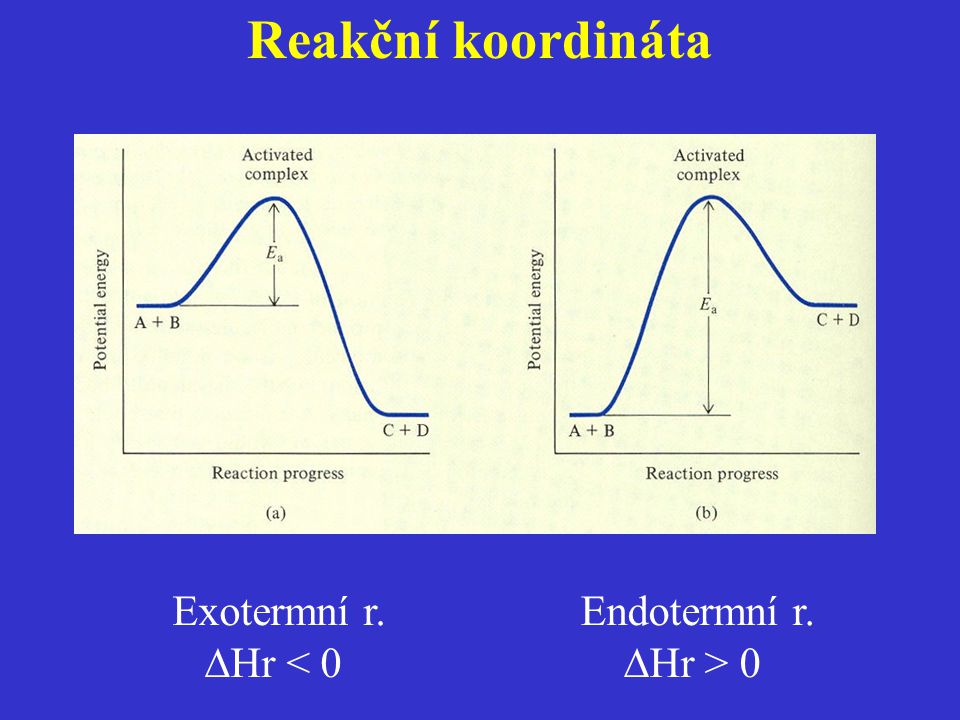
Reakce, při nichž dochází k uvolňování tepla jsou exo- termické, reakční teplo v tomto případě zapisujeme se záporným znaménkem. Reakce, při kterých se teplo spotřebovává, a tím pádem dochází k ochlazování, na- zýváme endotermické. Reakční teplo u endotermických reakcí zapisujeme s kladným znaménkem.
Co je to chemická rovnováha : Chemická rovnováha je takový stav soustavy, v němž se z makroskopického hlediska nemění její složení, i když v ní neustále probíhají chemické děje. Pokud budou v systému probíhat děje vratné, pak při rovnováze běží reakce oběma směry stejnou rychlostí.
Termochemie se zabývá studiem tepelného zabarvení chemických reakcí. Dle tepelného zabarvení dělíme reakce na exotermní (teplo se uvolňuje) a endotermní (teplo se spotřebovává). V termochemické rovnici se uvádí symboly skupenství u prvků či sloučenin, protože hodnoty reakčního tepla závisí i na skupenství. Hoření je fyzikálně chemická reakce, při které hořlavá látka reaguje vysokou rychlostí s oxidačním prostředkem za vzniku tepla a světla. Je to reakce exotermická.
Jak dělíme chemické reakce
Chemické reakce můžeme rozdělit dle různých kritérií, jako jsou například vnější změny, skupenství reaktantů, tepelné zabarvení (změna tepla v průběhu reakce) či typy přenášených částic.Chemická vazba
2.1 Kovová vazba.
2.2 Kovalentní vazba.
2.3 Iontová vazba.
Chemické reakce jsou děje, při kterých z výchozích látek (reaktantů) vznikají látky jiného složení (produkty); chemické reakce popisuje chemická rovnice. Chemická rovnice je symbolický zápis, kterým se popisuje výsledek chemické reakce ve stechiometricky správném poměru. Chemická rovnice vyjadřuje, které látky spolu reagují, které látky se rozkládají a které vznikají.
Co je dynamická rovnováha : Dynamická rovnováha je taková rovnováha, při které se nemění stav systému, avšak dochází k vnitřním změnám tohoto systému.
Co to je Termochemie : zabývá se tepelnými efekty při chemických reakcích a dějích jako je např. rozpouštění látek či skupenské přeměny. Děje – endotermické -jsou provázeny pohlcováním tepla, – exotermické – teplo se při nich uvolňuje.
Co to je chemické reakce
Chemické reakce jsou děje, při kterých z výchozích látek (reaktantů) vznikají látky jiného složení (produkty); chemické reakce popisuje chemická rovnice. Významnou vlastností dřeva (a obecně všech forem biomasy) je značný podíl takzvané prchavé hořlaviny. Při zahřátí na teplotu přes 200°C dochází k rozkladu a tvorbě hořlavých plynů. V důsledku toho, hoří dřevo dlouhým plamenem což trochu komplikuje konstrukci topenišť na jeho spalování.Chemické rovnice
Průběh chemické reakce se zapisuje chemickou rovnicí. Jednotlivé zúčastněné látky se oddělují znaménkem „+“, mezi výchozí látky a produkty reakce se zapisuje šipka (⟶). Rovnice výše lze přečíst takto: uhlík reaguje s dvouatomovou molekulou kyslíku (kyslíkem), vzniká oxid uhličitý.
Jak poznat typy vazeb : Obecně platí, že kovalentní vazby jsou mezi atomy dvou nekovových prvků (nekov-nekov), iontové vazby mezi kovem a nekovem (kov-nekov) a kovová vazba je mezi atomy kovů (kov-kov – v tomto případě se jedná o vysoký počet atomů kovu vzájemně sdílejících elektrony).
Antwort Co to je Endotermní reakce? Weitere Antworten – Co je to Endotermni reakce
Endotermická (endotermní) reakce (z řeckého ἔξω endo „dovnitř“ a θερμός thermós „teplý, horký, vyhřívaný“) je chemická reakce, při níž se energie spotřebovává, obvykle ve formě tepla. Produkty reakce proto mají vyšší chemickou energii než reaktanty, které do reakce vstoupily.Exotermická (exotermní) reakce (z řeckého ἔξω exo „venku“ a θερμός thermós „teplý, horký, vyhřívaný“) je chemická reakce, při níž se uvolňuje energie, obvykle ve formě tepla. Produkty reakce proto mají nižší chemickou energii než reaktanty, které do reakce vstoupily.Exotermní reakce
Jestliže se při chemické reakci uvolňuje teplo, hovoříme o reakci exotermní (exotermické). Exotermní reakce jsou mnohdy doprovázeny světelnými efekty či prudkým zvýšením teploty reakční směsi. Tyto reakce probíhají většinou samovolně, jejich nejběžnějším příkladem je hoření.

Jaké jsou typy chemických reakcí : Chemické reakce lze klasifikovat podle různých kritérií, včetně fyzikálního stavu substrátů a produktů nebo energetického účinku. Nejčastěji se však dělí podle typu a počtu složek, které se na nich podílejí a podle toho rozlišujeme reakce syntézní, rozkladné a vytěsňovací.
Jak se pozná Endotermická reakce
Reakce, při nichž dochází k uvolňování tepla jsou exo- termické, reakční teplo v tomto případě zapisujeme se záporným znaménkem. Reakce, při kterých se teplo spotřebovává, a tím pádem dochází k ochlazování, na- zýváme endotermické. Reakční teplo u endotermických reakcí zapisujeme s kladným znaménkem.
Co je to chemická rovnováha : Chemická rovnováha je takový stav soustavy, v němž se z makroskopického hlediska nemění její složení, i když v ní neustále probíhají chemické děje. Pokud budou v systému probíhat děje vratné, pak při rovnováze běží reakce oběma směry stejnou rychlostí.
Termochemie se zabývá studiem tepelného zabarvení chemických reakcí. Dle tepelného zabarvení dělíme reakce na exotermní (teplo se uvolňuje) a endotermní (teplo se spotřebovává). V termochemické rovnici se uvádí symboly skupenství u prvků či sloučenin, protože hodnoty reakčního tepla závisí i na skupenství.

Hoření je fyzikálně chemická reakce, při které hořlavá látka reaguje vysokou rychlostí s oxidačním prostředkem za vzniku tepla a světla. Je to reakce exotermická.
Jak dělíme chemické reakce
Chemické reakce můžeme rozdělit dle různých kritérií, jako jsou například vnější změny, skupenství reaktantů, tepelné zabarvení (změna tepla v průběhu reakce) či typy přenášených částic.Chemická vazba
Chemické reakce jsou děje, při kterých z výchozích látek (reaktantů) vznikají látky jiného složení (produkty); chemické reakce popisuje chemická rovnice.
Chemická rovnice je symbolický zápis, kterým se popisuje výsledek chemické reakce ve stechiometricky správném poměru. Chemická rovnice vyjadřuje, které látky spolu reagují, které látky se rozkládají a které vznikají.
Co je dynamická rovnováha : Dynamická rovnováha je taková rovnováha, při které se nemění stav systému, avšak dochází k vnitřním změnám tohoto systému.
Co to je Termochemie : zabývá se tepelnými efekty při chemických reakcích a dějích jako je např. rozpouštění látek či skupenské přeměny. Děje – endotermické -jsou provázeny pohlcováním tepla, – exotermické – teplo se při nich uvolňuje.
Co to je chemické reakce
Chemické reakce jsou děje, při kterých z výchozích látek (reaktantů) vznikají látky jiného složení (produkty); chemické reakce popisuje chemická rovnice.

Významnou vlastností dřeva (a obecně všech forem biomasy) je značný podíl takzvané prchavé hořlaviny. Při zahřátí na teplotu přes 200°C dochází k rozkladu a tvorbě hořlavých plynů. V důsledku toho, hoří dřevo dlouhým plamenem což trochu komplikuje konstrukci topenišť na jeho spalování.Chemické rovnice
Průběh chemické reakce se zapisuje chemickou rovnicí. Jednotlivé zúčastněné látky se oddělují znaménkem „+“, mezi výchozí látky a produkty reakce se zapisuje šipka (⟶). Rovnice výše lze přečíst takto: uhlík reaguje s dvouatomovou molekulou kyslíku (kyslíkem), vzniká oxid uhličitý.
Jak poznat typy vazeb : Obecně platí, že kovalentní vazby jsou mezi atomy dvou nekovových prvků (nekov-nekov), iontové vazby mezi kovem a nekovem (kov-nekov) a kovová vazba je mezi atomy kovů (kov-kov – v tomto případě se jedná o vysoký počet atomů kovu vzájemně sdílejících elektrony).